概述
双特异性抗体疗法所用药物以双管齐下的方式靶向治疗疾病。它采用双特异性抗体,是一种经专门设计、在实验室合成的蛋白质。
这类药物有多种剂型,作用方式也各不相同。许多双特异性抗体疗法属于免疫疗法,帮助人体的免疫系统识别并攻击癌细胞。其他类型则可阻断帮助癌细胞生长或存活的信号。它们的独特之处在于能够同时结合两种不同的蛋白质。常常是一种抗体与免疫细胞结合,另一种与癌细胞结合。双特异性抗体疗法有时简称双抗疗法或 BsAb。
多种双特异性抗体疗法已获得美国食品药品管理局(FDA)的批准。大多数用于治疗血液癌症和淋巴系统癌症,例如多发性骨髓瘤、白血病和淋巴瘤。少数获批用于治疗实体瘤,包括某些肺癌和眼癌。还有几种获批用于治疗非癌性状况,例如血友病和某些眼部疾病。
如果其他治疗失效,或许可以采用双特异性抗体疗法。该疗法也可能与其他治疗方法联合使用,以改善治疗效果。
双特异性抗体与单克隆抗体
双特异性抗体是单克隆抗体的升级版。单克隆抗体是天然抗体的合成替代品。它们靶向癌细胞上的单个蛋白质,增强人体对癌症的免疫应答。然而,虽然单克隆抗体可能在一段时间内有效,但癌细胞最终会通过其他方式逃避免疫攻击。
双特异性抗体有两个“臂”,可以同时与两种不同靶点相互作用,因而可以强效抵抗癌细胞。多特异性抗体目前也在研发中。
类型
双特异性抗体疗法:激活 T 细胞
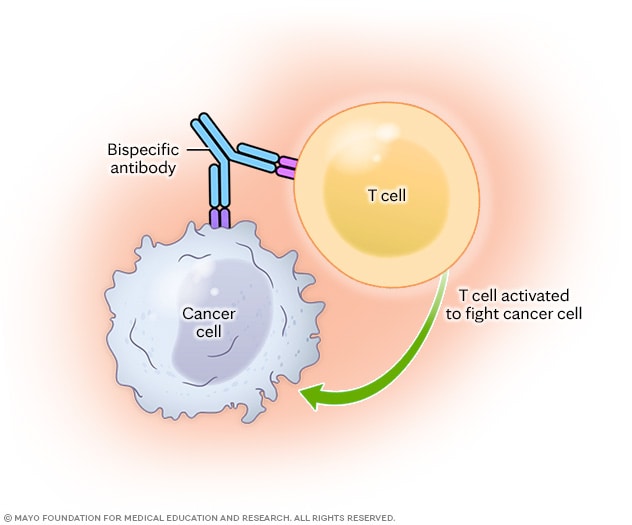
双特异性抗体疗法:激活 T 细胞
某些双特异性抗体疗法直接将免疫 T 细胞与癌细胞连接起来。双特异性抗体的一臂与 T 细胞连接,另一臂连接在癌细胞上。这种连接可以激活 T 细胞,释放蛋白质杀灭癌细胞。
双特异性抗体的作用机制因其设计方式而异。有数百种双特异性抗体正在进行临床试验,测试 60 多种不同的靶点组合。
常见类型包括:
- 激活免疫系统。 有些双特异性抗体直接把 T 细胞(关键免疫细胞)和癌细胞连接在一起。T 细胞通过攻击有害细胞来帮助保护身体。与 T 细胞相互作用的双特异性抗体有时被称为双特异性 T 细胞衔接器或 BiTE 疗法。双特异性抗体的一臂结合 CD3(一种激活 T 细胞的蛋白质复合物)。另一臂连接在癌细胞上。这种连接可以激活 T 细胞,释放蛋白质杀灭癌细胞。
- 阻断细胞信号。 有些双特异性抗体可以同时阻断两种细胞信号。例如,埃万妥单抗(Rybrevant)阻断两种可促进肺癌细胞生长的信号蛋白质:表皮生长因子受体(EGFR)和间质-上皮细胞转化因子(简称 MET,也被称为肝细胞生长因子受体)。阻断这些信号可以帮助减缓或阻止肿瘤生长。
- 精准治疗。 一些正在研究中的双特异性抗体用一臂结合癌细胞,另一臂则直接将药物或辐射递送至癌细胞。这种作用方式有助于将治疗性物质精准递送至治疗部位,这样或许可以减少对健康细胞的损伤。
双特异性抗体疗法的数个关键特征使之成为一种非常有吸引力的治疗方案。
- 即用疗法。 双特异性抗体是“现成”药物,因而不同于嵌合抗原受体(CAR)T 细胞疗法,后者需要定制化生产过程。
- 门诊治疗。 大多数患者不需要为了接受该治疗而在医院过夜。
- 副作用可管理。 发热或意识模糊之类的副作用通常比其他晚期癌症疗法要轻。
目的
双特异性抗体疗法主要用于治疗某些癌症,特别是在其他治疗方法(如化疗、靶向药物或 CAR-T 细胞疗法)不再有效的情况下。大多数双特异性抗体在专门的医疗中心通过静脉输注或注射给药。两种剂型均按周期给药。双特异性抗体研究进展迅速。其中有多种疗法正在进行临床试验。
在美国获批的双特异性抗体包括:
血液癌和淋巴系统癌症
- 贝林妥欧单抗(Blincyto)以 CD3 蛋白和 CD19 蛋白为靶向,从而连接免疫系统 T 细胞与白血病细胞。用于治疗急性淋巴母细胞白血病(ALL)。
- 特立妥单抗(Tecvayli)和埃纳妥单抗(Elrexfio)以 CD3 蛋白和 BCMA 蛋白为靶向,帮助破坏多发性骨髓瘤细胞。
- 塔奎妥单抗(Talvey)通过结合 CD3 蛋白和 GPRC5D 蛋白来治疗多发性骨髓瘤。
- 莫妥珠单抗(Lunsumio)和艾可瑞妥单抗(Epkinly)以 CD3 蛋白和 CD20 蛋白为靶向,治疗滤泡性淋巴瘤(一种生长缓慢的非霍奇金淋巴瘤)。
- 艾可瑞妥单抗(Epkinly)和格菲妥单抗(Columvi)还通过靶向 CD3 蛋白和 CD20 蛋白来治疗弥漫大 B 细胞淋巴瘤(DLBCL)和相关淋巴瘤。
实体瘤
- 埃万妥单抗(Rybrevant)通过结合 EGFR 蛋白和 MET 蛋白来治疗某些类型的非小细胞肺癌。
- 塔拉妥单抗(Imdelltra)通过靶向 CD3 蛋白和小细胞肺癌细胞上的 DLL3 蛋白来连接 T 细胞和癌细胞。
- 替本芙普(Kimmtrak)通过与免疫细胞上的 CD3 蛋白和肿瘤细胞上的 gp100 蛋白结合来连接 T 细胞和癌细胞,用于治疗葡萄膜黑色素瘤(一种罕见的眼部癌症)。
其他疾病
- 艾美赛珠单抗(Hemlibra)可与凝血因子 IXa 和凝血因子 X 蛋白结合,帮助预防 A 型血友病患者出血。
- 法瑞西单抗(Vabysmo)通过阻断 VEGF 和 Ang-2(这两种蛋白均与血管渗漏或病变有关),用于治疗黄斑变性、糖尿病性黄斑水肿和相关眼部疾病。
研究人员正在研究适用于早期癌症和其他实体瘤(例如肾癌和乳腺癌)的双特异性抗体。他们也在探索治疗方法的联合使用(例如双特异性抗体疗法与 CAR T 细胞疗法联用),以观察联合用药或序贯用药是否能改善治疗效果。
风险
与任何强效癌症疗法一样,双特异性抗体疗法也有引发副作用的风险。为了降低这种风险,双特异性抗体通常按剂量递增方案给药。这意味着您最初会接受较小剂量。之后,剂量会逐渐增加。您也可以提前使用其他药物,以帮助降低副作用风险。
双特异性抗体疗法的常见副作用包括:
细胞因子释放综合征
双特异性抗体疗法可能导致身体释放大量被称为细胞因子的炎性蛋白质。这种蛋白质的陡增可能导致一组被称为细胞因子释放综合征(CRS)的症状。该综合征通常发生在治疗初期,一般是在最初几次给药后。CRS 通常症状较轻且持续时间较短。但在某些情况下,症状可能会加重并可能危及生命。
轻度 CRS 可能会让您觉得自己得了流感。症状可能包括:
- 发热。
- 恶心。
- 寒战。
- 低血压。
- 头痛。
- 皮疹。
- 喉咙不适感。
- 呼吸困难。
- 心率加快。
医护团队会在给药后对您进行密切观察,可以及时发现这些症状,并立即给予治疗。
免疫效应细胞相关神经毒性综合征
炎症加重有时可能累及脑部或神经,导致一系列被称为免疫效应细胞相关神经毒性综合征(ICANS)的症状。该综合征有时被简称为神经毒性。
一般来说,这些变化是暂时的,在给药后数天到数周内出现。症状有轻有重。及早治疗会有助于逆转这些副作用。症状可能包括:
- 记忆力减退。
- 反应变慢。
- 意识模糊。
- 人格改变。
- 感觉疲倦。
- 意识丧失。
- 手足麻木。
- 难以集中注意力、言语困难或呼吸困难。
感染
双特异性抗体疗法的常见问题是感染风险增加。有以下几个相关原因:
- 免疫细胞减少。 双特异性抗体在攻击癌细胞的同时,也减少了健康免疫细胞的数量。其他免疫疗法(例如 CAR-T 细胞疗法)也可能发生这种情况。
- 有益抗体减少。 有些双特异性抗体可能会降低血液中免疫球蛋白的水平。免疫球蛋白是抵抗感染的抗体。
- 低血细胞计数。 强烈的免疫激活反应以及随之产生的细胞因子偏移可能会暂时降低骨髓功能。这可能导致某些白细胞计数降低。
这些因素可能降低抵抗细菌、病毒和真菌感染的能力。双特异性抗体治疗后常见的感染包括:
- 上呼吸道感染,例如普通感冒、流感和 2019 冠状病毒病(COVID-19)。
- 感染性肺炎。
- 尿路感染。
- 酵母菌感染。
有些感染可能会变严重。医护团队可能会给予您用于预防或治疗感染的药物。这可能包括直接将抗体注入血液,也被称为静脉注射免疫球蛋白(IVIg)。还可能包括抗生素、抗病毒药物和抗真菌药物。有些是按常规用药,有些则按需用药。
其他副作用
双特异性抗体疗法有时可能会在输注或注射后引起过敏反应,表现为皮疹和呼吸困难等症状。该疗法还可能引起肝功能变化,进而导致疲倦、食欲减退和黄疸。其他副作用可能包括皮肤干燥、指(趾)甲易碎和变色,以及口腔干燥。
双特异性抗体疗法可能会对胎儿造成伤害,因此不建议在怀孕期间使用。
如何进行准备
请向医疗护理团队咨询将会发生什么。您可能需要提前考虑的因素包括:
- 照护者支持。 在治疗早期和监测期间,您需要有人照护。
- 需要离家。 在治疗的第一阶段,您可能需要住在治疗机构附近。之后,您可能需要因持续治疗而往返奔波。
- 副作用。 在某些情况下,该疗法的副作用可能较严重。
- 费用较高。 请提前了解保险承保范围。
可能出现的情况
双特异性抗体疗法通常在医院或其他医疗机构提供。大多数患者可在手术当天出院回家。
与某些其他免疫疗法(如 CAR-T 细胞疗法)不同,双特异性抗体疗法并不是一次性治疗。该疗法需要定期给药,具体时间取决于您接受的治疗类型和您的个人需求。
术前
在您接受双特异性抗体药物治疗前,您的医护团队会建议您保持充足的水分。医护团队可能让您多喝水。对于某些双特异性抗体,医护团队还可能开出用于预防不良反应的药物,其中可能包括类固醇、抗组胺药或对乙酰氨基酚。
术中
治疗可通过两种方式进行:注射或静脉输注。
注射用双特异性抗体采用皮下注射给药。这使其吸收更为缓慢,时间较长。
治疗通常从小剂量开始,在数天到数周内逐渐增加剂量。这被称为阶梯式递增给药。通常每周治疗一次,如果六个月后治疗效果良好,有时会改为每两周治疗一次。
静脉输注直接将双特异性抗体注入静脉。抗体药物直接注入血液后可被快速吸收,立即对癌细胞发挥作用。
静脉输注可能持续最长 4 小时。第一次输注通常采用较小剂量,以降低发生副作用的风险。医护团队还可能给您其他药物,例如类固醇或补液,以帮助预防并发症。
静脉输注治疗通常采用阶梯式递增方案,在第 1 天、第 8 天和第 15 天给药。之后,一般每 1 至 3 周治疗一次,具体取决于治疗药物。
医护团队会进行密切监测,以观察您是否出现任何不良反应或副作用,特别是在第一次治疗后。该团队可以根据需要及时提供治疗。
术后
大多数患者可在接受治疗当天出院回家。医护团队会告知您回家后需要注意的事项。有些医院会提供一套设备,供您自行测量体温、血压和其他生命体征。这些测量结果以电子方式发送给医护团队进行远程监测。在家时,请记录您出现的症状。如有任何症状加重或任何异常症状,请立即告知医护团队。
持续使用双特异性抗体疗法期间经常发生感染。请采取以下措施降低出现并发症的风险:
- 控制症状。 如果出现感染体征,例如发热、寒战或疼痛加重(尤其是在止痛药无效的情况下),请立即告知医护团队。
- 接种合适的疫苗。 无论是您还是您身边的人,根据最新要求接种疫苗都很重要。请咨询您的医护团队,了解应该接种哪些疫苗以及何时接种。有些疫苗使用减毒活病毒或活细菌。这类疫苗对免疫系统功能低下者或其身边的人来说可能有失安全。但大多数常见疫苗都不是活疫苗,其中包括流感疫苗、COVID-19 疫苗、RSV 疫苗、肺炎球菌疫苗以及破伤风、白喉、百日咳联合疫苗(Tdap),因此免疫系统功能低下者可以安全使用。
- 尽量避免接触病菌。 采取额外措施以尽量减少病菌传播,会有所帮助。预防措施可能包括勤洗手、限制与病人接触以及避免食用未煮熟或生的食物。
某些双特异性抗体会引发独特的副作用。例如:
- 口腔干燥。
- 味觉丧失。
- 吞咽困难。
- 皮疹。
- 指甲变脆。
如果出现任何其他副作用,甚至是非预期作用,请告知医护团队。医护团队或许可以帮您找到缓解方法。
结果
在临床试验和真实世界研究中,双特异性抗体疗法均已帮助晚期癌症患者延长了生存期。即使在身体比较虚弱或者已接受过多种其他治疗的患者中,也观察到了这种益处。双特异性抗体还可以改善其他状况。例如,它们有助于降低血友病患者的出血风险。和您的医护团队交流,了解根据您的状况和正在接受的具体治疗,可以有什么样的预期。
临床试验
探索 Mayo Clinic 的研究 测试新的治疗、干预与检查方法,旨在预防、检测、治疗或控制这种疾病。