诊断
囊性纤维化常见问题解答
肺科医生 Sarah Chalmer 医学博士解答有关囊性纤维化的最常见问题。
大家好。我是妙佑医疗国际的肺脏学家 Sarah Chalmers 医生。现在我来解答一些大家可能关心的有关囊性纤维化的重要问题。
不能仅仅因为您宝宝的新生儿筛查呈阳性就认为其患有囊性纤维化。许多婴儿的筛查结果呈阳性,但实际上并未患有 CF。新生儿筛查检查的是血液中某种与囊性纤维化相关的物质是否升高,但是这种物质在其他情况下也可能升高,甚至早产也会导致这种现象。某些州还会检测基因突变,但即使检测结果呈阳性,也不表示您的宝宝患有这种疾病。只存在一个突变的人被称为携带者。这种人在美国十分常见,每 20 个人中就有一个是 CF 基因突变携带者。如果您宝宝的囊性纤维化筛查结果呈阳性,那需要带他们去看医生并进行汗液氯测试,以确定他们是否真的患有囊性纤维化。
事实上,CF 基因突变是由父母传给子女,这种特定遗传模式被称为常染色体隐性遗传。父母各自遗传一个 CF 基因给子女,因此每个人都有两个 CF 基因。这两个基因都存在突变才会发生这一疾病。只具有一个 CF 基因突变的人被称为携带者。如果父母之中有一人是携带者,那么他们有 50% 的几率将这个带突变基因遗传给子女。如果父母双方遗传给子女的都是正常基因,或者只有一方遗传了一个带突变基因,那么子女就不会患有 CF。如果父母双方遗传给子女的都是带突变基因,那么他们的子女将携带两个带突变的基因,并且极有可能会患上这种疾病。如果父母双方都是 CF 突变携带者,那么他们的每个子女患先天性囊性纤维化的几率均为 25%。
男性和女性都有可能患上囊性纤维化。但与男性相比,女性往往会发生更多症状和更频繁的肺部感染,并且她们往往在较小年龄就开始出现这些感染症状。这种现象的原因尚不明确。
事实上,将近 10% 的 CF 病例是在成年期确诊。您可能生来就患有囊性纤维化,但出于多种原因,这一疾病未能在儿童时期诊断出来。2010 年之前,一些州甚至没有安排囊性纤维化筛查。因此,如果您是在 2010 年之前出生的,那么您在婴儿时期可能没有接受过囊性纤维化新生儿筛检。某些基因突变引起的这一疾病非常轻微,并且可能到成年后才能察觉出症状。
CF 症状、疾病对患者器官以及患者生活产生的影响都因人而异。有些人病情非常轻微,只有一个器官受累,症状很少;而另一部分人则病情更为严重,症状更加棘手,并且有多个器官受累。包括基因突变类型在内的许多因素决定了这一疾病对患者的影响。但囊性纤维化护理团队会与每位患者单独合作,制定满足您个人需求的个性化治疗计划。
男性和女性囊性纤维化患者的生育能力都会受到影响。CF 女性患者的宫颈粘液增厚,而且月经周期也可能不规律。CF 女性患者的备孕时间可能更长。但大多数都能成功怀孕并且在怀孕期间正常生活,最终也能正常分娩。几乎所有 CF 男性患者都有不孕不育症。CF 男性患者能够产生正常精子,但输精管缺失。而因为他们仍然能产生精子,因此可利用辅助生殖技术来帮助这些男性 CF 患者获得亲生孩子。您的孩子是否患有 CF 取决于您和您的另一半遗传给孩子的基因组合,如果父母双方都没有基因突变,则患病概率为零,如果父母双方都患有 CF,则概率接近 100%。
请始终对医疗团队保持坦诚。请告知您正在服用哪些药物以及您的治疗频率。就诊前请写下您的所有问题,以便我们确保满足您的需求。感谢您的观看。祝您健康!
为诊断囊性纤维化,医生通常会对您进行体检、检查症状并进行多种检测。
新生儿筛检与诊断
现在美国每个州都会定期对新生儿进行囊性纤维化筛查。早期诊断意味着可以立即开始治疗。
在一项筛查测试中,检查由胰腺释放的免疫反应性胰蛋白酶原(IRT)是否高于正常水平。由于早产或分娩压力大,新生儿的 IRT 水平可能很高。因此,囊性纤维化的确诊可能需要其他检查。
为评估婴儿是否患有囊性纤维化,医生可能会在婴儿至少 2 周大时进行汗液试验。将一种能产生汗液的化学物质涂在小块皮肤上。随后收集汗液进行检测,看看含盐量是否比正常情况更高。在囊性纤维化基金会认可的护理中心进行的检测的结果更可靠。
医生可能还会建议对导致囊性纤维化的基因的特定缺陷进行基因检测。除检查 IRT 水平外,也可以使用基因检测来确认诊断。
大龄儿童和成人的检查
对于出生时未做筛查的大龄儿童和成人,可能会建议进行囊性纤维化检查。如果您出现反复发作的胰腺发炎、鼻息肉、慢性鼻窦或肺部感染、支气管扩张或男性不育症,医生可能建议进行 CF 的遗传学和汗液检查。
治疗
囊性纤维化尚无治愈方法,但通过治疗可以减轻症状、减少并发症并改善生活质量。建议通过密切监测和积极的早期干预来减缓囊性纤维化进展,从而延长寿命。
囊性纤维化的治疗非常复杂,因此在选择治疗中心时,应考虑选择在囊性纤维化诊疗方面接受过培训的医生或医学专家组成的多学科团队,由他们来负责您的治疗。
治疗目标包括:
- 预防和控制肺部感染
- 清除和溶解肺内黏液
- 治疗和预防肠道阻塞
- 提供充足的营养
药物
治疗选择包括:
- 靶向基因突变的药物,包括一种新型药物,它组合了三种药物来治疗引起囊性纤维化(CF)的最常见基因突变,被认为是治疗上的重大成果
- 治疗和预防肺部感染的抗生素
- 减轻肺部气道内肿胀的抗炎药物
- 痰液稀释药物,例如高渗盐水,帮助您咳出痰液,从而改善肺部功能
- 叫做支气管扩张剂的吸入药物通过放松支气管周围的肌肉帮助保持气道开放
- 口服胰酶帮助消化道吸收营养
- 大便软化剂来预防便秘或肠梗阻
- 降酸药物促进胰酶效果
- 治疗糖尿病或肝病的特定药物(视需要)
靶向基因的药物
对于存在某种基因突变的囊性纤维化患者,医生可能会建议使用囊性纤维化跨膜电导调节剂 (CFTR)。这类新型药物有助于改善有缺陷的 CFTR 蛋白质的功能。它们可改善肺功能和体重,并减少汗液中的含盐量。
FDA 已批准这些药物用于治疗存在一个或多个 CFTR 基因突变的 CF 患者:
- 含有 elexacaftor、依伐卡托和替扎卡托的最新组合药物(Trikafta)获批准用于治疗 12 岁及以上的患者,被许多专家认为是重大突破。
- 含有替扎卡托和依伐卡托的复方药物(Symdeko)获批准用于治疗 6 岁及以上的患者。
- 含有鲁马卡托和依伐卡托的复方药物(Orkambi)获批准用于治疗 2 岁及以上患者。
- 依伐卡托 (Kalydeco) 已获批用于治疗 6 月龄及以上的患者。
针对囊性纤维化的里程碑式治疗方法
Tim Myer 生来患有囊性纤维化 (CF)。当他在等待肺移植手术时,美国食品和药品管理局批准的一种新药改变了一切。Myer 和他在妙佑医疗国际的肺科医生 Mark Wylam 共同分享这个值得纪念的故事。
妙佑医疗国际问答播客
在开具这些药物之前,医生可能会进行肝功能检测和眼科检查。在服用这些药物的同时,还需要定期进行检测,以确定是否有肝功能异常和白内障等副作用。向医生和药剂师咨询可能的副作用和注意事项。
保持定期复诊,这样医生就可以在您服用这些药物期间对您进行监测。告知医生出现的所有副作用。
气道廓清技术
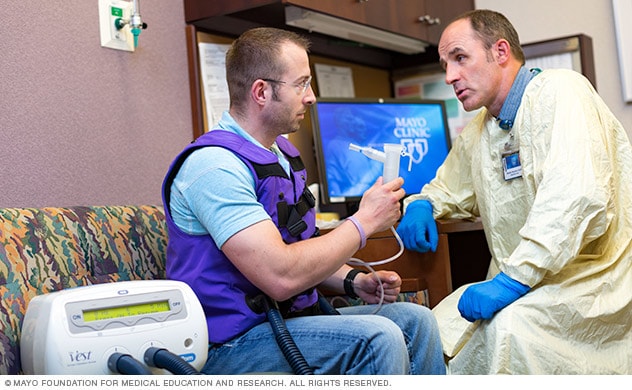 背心疗法
背心疗法
妙佑医疗国际的呼吸治疗师采用定制疗法,与一位囊性纤维化成人患者讨论充气背心疗法。
气道廓清技术,也称为胸部物理治疗(CPT),可以减轻黏液阻塞,并有助于降低气道中的感染和炎症。这些技术可缓解肺部黏稠的黏液,更容易咳嗽。
气道廓清技术通常需要每天进行多次。可以使用不同类型的 CPT 缓解并清除黏液,可能推荐采用多种技术联合的方法。
- 常见手段是空心掌叩击胸部的正面和背面。
- 一些呼吸和咳嗽技术也可能有助于缓解黏液。
- 机械装置能够帮助缓解肺黏液。设备包括一个可以吹气的管子和将空气脉冲至肺部的机器(背心式振动排痰机)。剧烈运动也可能会用于清除黏液。
医生将指导您接受最适合您的胸部物理治疗的类型与频率。
肺康复治疗
医生可能会提出一项长期计划,以改善您的肺功能和总体健康状况。肺康复治疗通常在门诊部完成,可能包括:
- 体育锻炼,以改善病情
- 呼吸技巧,以帮助稀释黏液和改善呼吸
- 营养咨询
- 咨询和支持
- 病情相关教育
外科手术及其他医疗操作
针对由囊性纤维化引起的某些疾病的治疗方案包括:
临床试验
探索 Mayo Clinic 的研究 测试新的治疗、干预与检查方法,旨在预防、检测、治疗或控制这种疾病。
生活方式与家庭疗法
有几种方法可以控制症状并尽量减少并发症。
注意营养和水分摄入
囊性纤维化会导致营养不良,因为消化酶不能到达小肠,从而阻碍食物的吸收。CF 患者每日所需卡路里量可能远高于健康人。
健康的饮食对生长发育和维护肺功能很重要。多喝水也很重要,这有助于稀释您肺部的黏液。您可与营养师一起制定营养计划。
医生可能会建议:
- 吃正餐和零食时同时服用胰酶胶囊
- 抑制胃酸分泌的药物
- 补充高热量的营养
- 特殊的脂溶性维生素
- 多吃纤维以防止肠阻塞
- 补充盐分,尤其是在炎热的天气或运动前
- 摄入充足的水分,尤其是在炎热的天气
按时接种疫苗
除接受其他常见的儿童期疫苗外,囊性纤维化患者还应接种年度流感疫苗和医生建议的任何其他疫苗,例如预防感染性肺炎的疫苗。CF 不会影响免疫系统,但患有 CF 的儿童在生病时更易出现并发症。
运动
定期运动有助于松解气道内的黏液并增强心脏功能。由于囊性纤维化患者现在活得更久,维持心血管健康对于健康生活非常重要。任何能让您运动起来的事情(包括步行和骑自行车)都会有帮助。
消除烟雾
不要抽烟,也不要让别人在您或您的孩子周围抽烟。二手烟对每个人都有害,尤其是对囊性纤维化患者,就像空气污染一样。
鼓励洗手
教导家人在吃饭前、如厕后、下班回家或放学回家时、与患病者共处后,应彻底洗手。洗手是预防感染的最佳方法。
前去就诊
您将得到医生和其他专业医护人员的持续护理。
- 确保参加您的定期随访。
- 按处方服药并遵医嘱进行治疗。
- 向医生咨询如何处理症状和严重并发症的警告信号。
妥善处理与支持
如果您或您的亲友患有囊性纤维化,您可能会出现强烈的情绪,如抑郁、焦虑、愤怒或恐惧。这些问题在青少年中尤为常见。以下建议可能会有所帮助。
- 寻求支持。开诚布公地谈论您的感受会有所帮助。与其他存在同样问题的人交流也会有所裨益。这可能意味着,自己加入一个互助组,或者为子女患有囊性纤维化的父母找到一个互助组。年纪稍长的囊性纤维化患儿可能希望加入囊性纤维化小组,与其他患有相同疾病的人见面并交谈。
- 寻求专业帮助。如果您或您的孩子感到抑郁或焦虑,咨询心理健康专家可能有所帮助。专家可以与您探讨感受和应对策略,也可以提供药物或其他治疗建议。
- 与家人朋友共度时光。他们的支持可以帮助您管理压力,减少焦虑。必要时向朋友或家人寻求帮助。
- 花点时间去了解囊性纤维化。如果您的孩子患有囊性纤维化,鼓励他们去了解囊性纤维化。获悉随着孩子长大成人,如何管理囊性纤维化患者的医疗护理。如果存在护理疑问,请咨询医生。
准备您的预约
如果您或您的孩子有囊性纤维化的常见体征或症状,请预约医生就诊。初步评估后,您可能会被转诊给在囊性纤维化评估和治疗方面训练有素的医生。
以下信息可以帮助您做好就诊准备,并了解医生可能做什么。
您可以做什么
您应该准备以下问题的答案:
- 您或您的孩子有什么症状?
- 症状是从什么时候开始的?
- 有什么因素能使症状好转或恶化吗?
- 您家里有人曾出现过囊性纤维化吗?
- 发育是否正常,体重是否稳定?
医生可能做些什么
获得关于症状以及您家族病史的详细信息后,医生可能会安排检测以帮助诊断和规划治疗。
Nov. 23, 2021