نظرة عامة
العلاج الإشعاعي
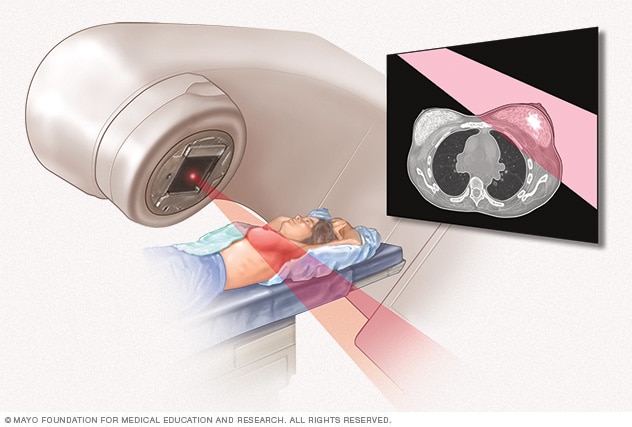
العلاج الإشعاعي
تستخدم الحزم الإشعاعية الخارجية إشعاعًا عالي الطاقة للقضاء على خلايا السرطان. ويستهدف الإشعاع بدقة السرطان باستخدام جهاز يتحرك حول جسم المريض.
يستخدم العلاج الإشعاعي لسرطان الثدي الأشعة السينية عالية الطاقة أو البروتونات أو الجسيمات الأخرى لقتل الخلايا السرطانية. وتتسم الخلايا سريعة النمو -مثل الخلايا السرطانية- بأنها أكثر قابلية لتأثيرات العلاج الإشعاعي من الخلايا الطبيعية.
لا تسبب الأشعة السينية أو الجسيمات ألمًا، ولا يمكن رؤيتها. لن تكوني مُشعة بعد العلاج، ولهذا فلا بأس من الوجود بجانب أشخاص آخرين بما في ذلك الأطفال.
يمكن توصيل العلاج الإشعاعي لسرطان الثدي من خلال:
- الإشعاع الخارجي. ينقل الجهاز الإشعاع من خارج جسمك إلى الثدي. وهذا هو النوع الأكثر شيوعًا من العلاج الإشعاعي المستخدم لسرطان الثدي.
- الإشعاع الداخلي (العلاج الإشعاعي الداخلي). بعد الخضوع لجراحة استئصال السرطان، يضع الطبيب بصورة مؤقتة جهازًا لتوصيل الإشعاع في ثديك إلى المنطقة التي كانت مصابة بالسرطان. ويضع مصدرًا مشعًا داخل الجهاز لفترات زمنية قصيرة خلال فترة العلاج.
يمكن أن يُستخدم العلاج الإشعاعي لعلاج سرطان الثدي في كل مراحله تقريبًا. والعلاج الإشعاعي من الطرق الفعالة في تقليل فرص تكرار الإصابة بسرطان الثدي بعد الجراحة. وهو يُستخدم أيضًا عادةً لتخفيف الأعراض الناتجة عن السرطان الذي انتشر إلى أجزاء أخرى من الجسم (سرطان الثدي النقيلي).
المنتجات والخدمات
لماذا تُجرى
يعمل العلاج الإشعاعي على قتل الخلايا السرطانية. وغالبًا ما يُستخدَم بعد الجراحة لتقليل خطر عودة السرطان. ويمكن استخدامه أيضًا لتخفيف الألم والأعراض الأخرى الناتجة عن سرطان الثدي المتقدم.
الإشعاع بعد استئصال الورم
إذا كنتِ ستخضعين لعملية لإزالة سرطان الثدي مع الحفاظ على باقي أنسجة الثدي سليمة (استئصال الكتلة الورمية أو جراحة الثدي المحافظة)، فقد يوصي طبيبك باستخدام الإشعاع بعد العملية لقتل أي خلايا سرطانية قد تكون متبقية. حيث تقلل إضافة الإشعاع بعد استئصال الكتلة الورمية من خطر عودة السرطان في الثدي المصاب.
ويُشار غالبًا إلى الجمع بين العلاج الإشعاعي واستئصال الكتلة الورمية بعلاج الحفاظ على الثدي. وتساوى فاعلية هذا النوع من العلاج فاعلية إزالة نسيج الثدي بالكامل (استئصال الثدي). وفي الحالات الخاصة التي يكون فيها خطر تكرار الإصابة منخفضًا جدًا، قد يناقش طبيبكِ أيضًا خيار تجنب الإشعاع بعد استئصال الكتلة الورمية.
بعد استئصال الكتلة الورمية، قد تشمل خيارات العلاج الإشعاعي ما يلي:
- تعريض الثدي بالكامل للإشعاع. أحد أكثر أنواع العلاج الإشعاعي المستخدمة بعد استئصال الكتلة الورمية شيوعًا هو تعريض الثدي بالكامل للحزم الإشعاعية الخارجية (العلاج الإشعاعي للثدي بالكامل).
- تعريض جزء من الثدي للإشعاع. قد يكون العلاج الإشعاعي لجزء من الثدي (العلاج الإشعاعي الجزئي للثدي) خيارًا مناسبًا لبعض أنواع سرطانات الثدي في المراحل الأولى. وتوجه هذه التقنية إشعاعًا خارجيًا أو داخليًا إلى المنطقة المحيطة بالمكان الذي تم استئصال السرطان منه.
الإشعاع بعد استئصال الثدي
يمكن استخدام العلاج الإشعاعي أيضًا بعد استئصال الثدي. وفي هذه الحالة، يمكن للإشعاع تدمير أي خلايا سرطانية قد تكون متبقية وتقليل خطر عودة السرطان في الأنسجة المتبقية من جدار الصدر أو العقد اللمفية.
عند تحديد ما إذا كان ينبغي لكِ الخضوع للإشعاع بعد استئصال الثدي أم لا، سيفكر الطبيب فيما إذا كان لديكِ:
- عُقَد لمفية بها مؤشرات على سرطان الثدي. العُقَد اللمفية تحت الإبط (الإبطية) التي تُظهر نتائج إيجابية في اختبار الخلايا السرطانية تكون مؤشرًا على انتشار بعض الخلايا السرطانية خارج الثدي.
- حجم الورم كبير. عادةً ما يكون الورم الأكبر من بوصتين (5 سنتيمترات) تقريبًا أكثر عرضة للعودة مرة أخرى مقارنةً بالأورام الأصغر حجمًا.
- حواف أنسجة بها مؤشرات على سرطان الثدي. بعد استئصال أنسجة الثدي، يُجرى فحص حواف الأنسجة بحثًا عن مؤشرات وجود خلايا سرطانية. وتمثل الحواف الضيقة للغاية أو الحواف التي تكون نتائجها إيجابية في اختبار وجود خلايا سرطانية أحد عوامل الخطورة لتكرار الإصابة.
الإشعاع لعلاج سرطان الثدي المتقدم الموضعي
يمكن أيضًا استخدام العلاج الإشعاعي لعلاج ما يلي:
- سرطانات الثدي التي لا يمكن استئصالها جراحيًا.
- سرطان الثدي الالتهابي، وهو نوع نشط من السرطان ينتشر في القنوات اللمفية للجلد الذي يغطي الثدي. ويعالَج هذا النوع من السرطان عادة بالعلاج الكيميائي قبل استئصال الثدي، ويتبع ذلك الإشعاع لتقليل فرصة تكرار الإصابة.
الإشعاع للتعامل مع سرطان الثدي الانتقالي
إذا انتشر سرطان الثدي في أجزاء أخرى من الجسم، فقد يُوصى بالعلاج الإشعاعي لتقليص حجم الورم والمساعدة على تخفيف الأعراض مثل الألم.
المخاطر
تختلف الآثار الجانبية للعلاج الإشعاعي اختلافًا كبيرًا اعتمادًا على نوع العلاج وعلى الأنسجة التي تتعرض للإشعاع. وتصل الآثار الجانبية إلى ذروتها في نهاية العلاج الإشعاعي. بعد الانتهاء من الجلسات، قد تختفي الآثار الجانبية في غضون عدة أيام أو أسابيع.
وقد تتضمن الآثار الجانبية الشائعة خلال فترة العلاج ما يلي:
- الإرهاق البسيط أو المتوسط
- تهيج الجلد، مثل الشعور بحكة أو احمرار أو تقشير أو تقرح، على غرار ما يحدث مع حروق الشمس
- تورم الثدي
واعتمادًا على الأنسجة التي تخضع للعلاج، قد يؤدي العلاج الإشعاعي إلى زيادة خطر الإصابة بالأعراض التالية أو التسبب في حدوثها:
- تورم الذراع (الوذمة اللمفية) إذا كانت العُقَد اللمفية الموجودة تحت الذراع مستهدفة بالعلاج
- الأضرار أو المضاعفات التي تؤدي إلى إزالة الغرسة إذا كنتِ قد خضعتِ لإعادة بناء الثدي باستخدام غرسة بعد استئصال الثدي
وفي حالات نادرة، قد يؤدي العلاج الإشعاعي إلى زيادة خطر الإصابة بالأعراض التالية أو التسبب في حدوثها:
- كسر في الضلوع أو ألم عند لمس جدار الصدر
- التهاب أنسجة الرئة أو إلحاق ضرر بالقلب
- الإصابة بأنواع ثانوية من السرطان، مثل سرطان العظام أو سرطان العضلات (الساركومة) أو سرطان الرئة
كيف تستعد
قبل الخضوع للعلاجات الإشعاعية، ستلتقي بفريق العلاج الإشعاعي الذي قد يشمل:
- اختصاصي علاج الأورام بالإشعاع، وهو طبيب متخصص في علاج السرطان بالإشعاع. يحدد اختصاصي علاج الأورام بالإشعاع العلاج المناسب لك ويتابع تحسنك ويعدل العلاج الذي تتناوله عند الحاجة.
- اختصاصي فيزياء طب علاج الأورام بالإشعاع وقياس الجرعات، وهو الذي يجري الحسابات والقياسات المتعلقة بجرعة الإشعاع وتوصيلها.
- ممرض علاج الأورام بالإشعاع أو ممرض ممارس أو مساعد طبيب، وهو الذي يجيب الأسئلة المتعلقة بالعلاجات والآثار الجانبية ويساعدك على الاهتمام بصحتك أثناء العلاج.
- اختصاصي العلاج بالإشعاع، وهو الذي يشغل معدات الإشعاع ويعطيك علاجاتك.
قبل أن تبدأ العلاج، سيراجع اختصاصي علاج الأورام بالإشعاع تاريخك المرضي معك ويُجري لك فحصًا بدنيًا لتحديد ما إذا كنت ستستفيد من العلاج الإشعاعي أم لا. وسيناقش الطبيب الفوائد المحتملة والآثار الجانبية لخضوعك للعلاج الإشعاعي.
قبل العلاج الإشعاعي الخارجي
قبل جلسة العلاج الأولى، ستخضعين لجلسة تخطيط العلاج الإشعاعي (المحاكاة) التي يفحص فيها اختصاصي الأورام بالإشعاع منطقة الثدي بعناية لتحديد الموقع المحدد الذي سيخضع للعلاج. خلال المحاكاة:
- يساعدكِ اختصاصي العلاج بالإشعاع على تحديد أفضل وضع مناسب لاستهداف المنطقة المصابة وتجنب الإضرار بالأنسجة السليمة المحيطة. وتُستخدم وسائد أو أدوات أخرى في بعض الأحيان لمساعدتك على الثبات في هذا الوضع.
- ستجرين فحصًا بالتصوير المقطعي المحوسب حتى يمكن لاختصاصي علاج الأورام بالإشعاع تحديد منطقة العلاج والأنسجة السليمة لتفاديها. ستسمعين ضوضاء من جهاز الفحص بالتصوير المقطعي المحوسب أثناء تحركه من حولك. حاولي الاسترخاء والثبات قدر الإمكان للمساعدة على ضمان دقة العلاج وانتظامه.
- قد يضع اختصاصي العلاج الإشعاعي علامات على جسمك بحبر شبه دائم أو بنقاط وشم دائمة صغيرة. وستوجه هذه العلامات اختصاصي العلاج الإشعاعي في استخدام الإشعاع. ينبغي توخي الحذر عند الغسل لتجنب فرك هذه العلامات وإزالتها.
- يستخدم اختصاصي قياس الجرعات واختصاصي فيزياء الإشعاع واختصاصي علاج الأورام بالإشعاع برامج الكمبيوتر للتخطيط للعلاج الإشعاعي الذي ستتلقينه. يمكنك البدء في العلاج بمجرد اكتمال المحاكاة والتخطيط وإتمام فحوصات ضمان الجودة المتعددة.
قبل المعالجة الإشعاعية الداخلية
قبل بدء المعالجة الإشعاعية الداخلية (المعالجة الكَثَبِيّة)، يوضع جهاز خاص لوضع المادة المشعة في المنطقة التي تم استئصال الورم السرطاني منها. ويمكن القيام بذلك أثناء جراحة السرطان أو كإجراء منفصل بعد عدة أيام.
ما يمكنك توقعه
عادة ما يبدأ العلاج الإشعاعي بعد الجراحة بمدة من ثلاثة إلى ثمانية أسابيع، إلا إذا كان هناك تخطيط للعلاج الكيميائي. وفي حال كان هناك تخطيط للعلاج الكيميائي، فعادةً ما يبدأ العلاج الإشعاعي بعد ثلاثة أو أربعة أسابيع من انتهاء العلاج الكيميائي. ستتلقين العلاج الإشعاعي على الأرجح في العيادات الخارجية في المستشفى أو مرفق علاجي آخر.
يتضمن الجدول العلاجي الشائع (مسار العلاج) جلسة علاج إشعاعي واحدة في اليوم لمدة خمسة أيام في الأسبوع (عادةً من الاثنين إلى الجمعة) ويستمر ذلك لخمسة أو ستة أسابيع. لا يزال هذا المسار العلاجي مستخدمًا بشكل شائع مع الأشخاص الذين يحتاجون إلى إشعاع العقد اللمفية.
يوصي الأطباء كثيرًا بجداول علاج أقصر (العلاج الإشعاعي بطريقة التجزئة المكثفة). يمكن تقليل فترة العلاج الإشعاعي للثدي بالكامل في كثير من الأحيان بحيث تستغرق من أسبوع إلى أربعة أسابيع. قد ينتهي العلاج الإشعاعي الجزئي للثدي في خلال خمسة أيام أو أقل. تؤدي جداول العلاج بالتجزئة المكثفة هذه الوظيفة نفسها التي تؤديها الجداول التي تستغرق وقتًا أطول وقد تقلل من خطر بعض الآثار الجانبية. ويمكن أن يساعد اختصاصي علاج الأورام بالإشعاع على تحديد المسار العلاجي المناسب لحالتك.
أثناء الإشعاع الخارجي
عادةً ما تتبع جلسة العلاج الإشعاعي الخارجي النموذجية هذا التسلسل:
- عندما تصلين إلى المستشفى أو منشأة العلاج، ستُنقَلين إلى غرفة خاصة تُستخدم خصوصًا للعلاج الإشعاعي.
- قد تحتاجين إلى خلع ملابسكِ وارتداء ثوب المستشفى.
- يساعدك المعالج بالإشعاع على الوصول إلى الوضع الذي كنت فيه أثناء عملية المحاكاة.
- قد يلتقط المعالج صورًا أو أشعة سينية للتأكد من أنك في وضع صحيح.
- يغادر المعالج الغرفة ويشغل الآلة التي تنقل الإشعاع (المسرّع الخطي).
- سيكون المعالج غير موجود في الغرفة أثناء العلاج، إلا أنه سيراقبك من غرفة أخرى عبر شاشة تليفزيونية. عادة ما يمكنك أنت والمعالج التحدث معًا عبر جهاز اتصال داخلي. إذا شعرت بالتعب أو عدم الارتياح، فأخبري المعالج، الذي يمكنه إيقاف العملية إذا لزم الأمر.
قد يستغرق توصيل الإشعاع بضع دقائق فقط، لكن توقعي قضاء من 15 إلى 45 دقيقة لكل جلسة، حيث قد يستغرق إعدادك في الوضع نفسه كل يوم عدة دقائق. وتضمن هذه الخطوة تقديم علاج إشعاعي دقيق.
العلاج الإشعاعي غير مؤلم. ولكنك قد تشعرين ببعض الانزعاج من الاستلقاء في الوضعية المطلوبة، لكن هذا لن يستغرق إلا وقتًا قصيرًا في العموم.
بعد الجلسة، لكِ الحرية في ممارسة أنشطتك المعتادة. التزمي بأي خطوات رعاية ذاتية في المنزل يوصي بها طبيبك أو ممرضتك، مثل العناية بالجلد.
في بعض الحالات، قد يوصي طبيبك بتعزيز الإشعاع فور الانتهاء من جلسات العلاج الإشعاعي الرئيسية. ويستغرق ذلك عادةً من أربعة إلى خمسة أيام إضافية ويمكن تجزئة الإشعاع على دفعات وتوجيهه إلى المكان الذي يمثل مصدر القلق الأكبر. على سبيل المثال، بعد استكمال العلاج الإشعاعي للثدي بالكامل، عادةً ما تُعطى المنطقة التي تمت إزالة السرطان منها تعزيزًا إشعاعيًا.
أثناء الإشعاع الداخلي
في حالة الإشعاع الداخلي، يتم إدخال المصدر المُشع داخل جهاز توصيل الإشعاع المزروع مرة أو مرتين يوميًا لبضع دقائق. ويُجرى ذلك عادةً دون مبيت في المستشفى، ويمكنك المغادرة بين الجلسات.
وبعد فترة العلاج، يُزال جهاز توصيل الإشعاع. وقد تحصل على مُسكنات للألم قبل هذا الإجراء. قد تشعر بوجع أو ألم عند لمس المنطقة لعدة أيام أو أسابيع أثناء تعافي الأنسجة من الجراحة والإشعاع.
النتائج
بعد الانتهاء من العلاج الإشعاعي، سيحدد اختصاصي علاج الأورام بالإشعاع أو غيره من المهنيين الطبيين مواعيد زيارات المتابعة لمتابعة مدى تحسن حالتك والبحث عن الآثار الجانبية المتأخرة والتحقق من مؤشرات المرض المتعلقة بتكرار الإصابة بالسرطان. أعدّي قائمة بالأسئلة التي ترغبين في طرحها على فريق الرعاية.
بعد الانتهاء من العلاج الإشعاعي، أخبري الطبيب في حال الشعور بأي مما يلي:
- ألم مستمر
- ظهور كتل أو كدمات أو طفح أو تورم مؤخرًا
- فقدان وزن غير مبرر
- حمى أو سعال بشكل متواصل
- أي أعراض أخرى تزعجك
التجارب السريرية
استكشِف دراسات مايو كلينك حول الاختبارات والإجراءات المخصصة للوقاية من الحالات الصحية واكتشافها وعلاجها وإدارتها.